Cenni teorici
La salinità è uno dei parametri fondamentali e più misurati dell’acqua di mare. Da essa dipendono diverse proprietà dell’acqua di mare, tra cui la densità, la conducibilità e il punto di congelamento. E’ inoltre un fattore ecologico di considerevole importanza, in grado di influenzare la tipologia di organismi che vivono in un corpo idrico.
La salinità dell’acqua di mare dipende dalla concentrazione di 11 ioni detti costituenti maggiori (Tabella). Di fatto si tratta degli elementi chimici presenti con concentrazione maggiore di 1 ppm (1 mg in 1 kg). Come si può osservare il maggior contributo è dato da Cl- e Na+.
Il valore medio della salinità oceanica superficiale è pari a ~35 g kg-1 (‰), ma varia tra ~34 e ~38 ‰, a seconda degli apporti di acqua per precipitazioni atmosferiche, fiumi, fusione del ghiaccio in zone polari e dell’evaporazione.
La determinazione della salinità di un campione di acqua di mare (contenuto totale di ioni disciolti) sfrutta il fatto che il rapporto tra i principali costituenti è praticamente costante e può essere fatta a partire dalla misura di clorinità. Per clorinità si intende il contenuto totale degli alogenuri, cioè cloruro (Cl-), bromuro (Br-) e ioduro (I-) del campione.
La relazione tra salinità e clorinità (entrambe espresse in g kg-1 (‰) )è la seguente:
S(‰)= 1.80655 Cl(‰)
La clorinità si determina con il metodo di Mohr (metodo argentometrico), ovvero una titolazione che sfrutta la precipitazione degli alogenuri ad opera del nitrato d’argento:
AgNO3(aq) + Cl- -> AgCl(s) + NO3-
AgNO3(aq) + Br- -> AgBr(s) + NO3-
AgNO3(aq) + I- -> AgI(s) + NO3-
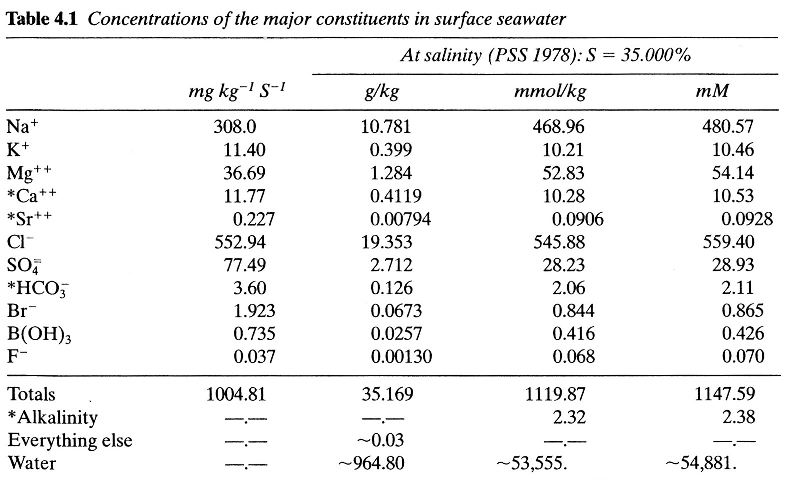
Costituenti maggiori e loro concentrazione in un campione di acqua di mare con salinità media 35 ‰
Materiali
campione di acqua di mare, cilindro graduato, matraccio (100 mL), bilancia, pipetta graduata (10 mL) per il prelievo dell’acqua da titolare, beuta (250 mL), pipetta graduata (10 mL) per titolare, beaker (50 o 100 mL) per contenere AgNO3, AgNO3 0.1 M, K2CrO4 al 5%
Procedimento:
- Trasferire 20mL di acqua di mare in matraccio da 100mL, registrandone il peso. Portare a volume con acqua distillata.
- Aspirare esattamente 10mL di soluzione diluita e trasferire in beuta. Aggiungere 50 mL di acqua distillata (misurata con cilindro).
- Prelevare una pipettata (~2mL) di K2CrO4 al 5% come indicatore e aggiungerli al campione da titolare.
- Aspirare esattamente 10mL di soluzione standard di AgNO3 0.1 M con la pipetta graduata.
- Titolare con la soluzione prelevata fino alla prima variazione cromatica dovuta alla precipitazione di Ag2CrO4.
- Registrare il volume di AgNO3 aggiunto:...
Sulla base della teoria di cui sopra, calcola S(‰) del campione.

